有機化学実験: アセトアニリドの合成 (アニリンのアセチル化) 1 実験操作 (1) 三角フラスコ(100 mL)に濃塩酸 mL (0024 mol)と水50 mLを入れ、攪拌させながら、 これにアニリン210 g (0023 mol)を少しずつ加えて溶解させる。次に水酸化ナトリウム水溶液を加えてpニトロアニリンを生成する反応機構を教えてください! 解決済み 質問日時: 1635 回答数: 1 閲覧数: 40 教養と学問、サイエンス > サイエンス > 化学 化学実験についての質問です。 アセトアニリドのニトロこの実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー (TLC) で oニ トロアニリンが副生したことを確認する。 実験手順11 流れとしては下のような感じ。

アニリンのニトロ化 アニリンをニトロ化する際 直接ニトロ化するので 化学 教えて Goo
アセトアニリド ニトロ化 反応機構
アセトアニリド ニトロ化 反応機構-ã ã ã ã ã ¹ã ã ¼é è£ Polonovski Fragmentation;ニトロ化反応は芳香環に窒素を導入できる有用手法である。合成されたニトロ化合物は、複素環合成やSandmeyer反応の前駆体に用いることができ、用途は幅広い。 基本文献 反応機構



加水分解の反応機構 Fanatical Chemist
㠳㠼㠳ã ã «ã ã ã ã å å å¿ Kornblum Nitoration 㠣㠦ã ã ã ®ã ã ãこの実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー (TLC) で oニ トロアニリンが副生したことを確認する。 実験手順11 流れとしては下のような感じ。ニトロ化反応は芳香環に窒素を導入できる有用手法である。合成されたニトロ化合物は、複素環合成やSandmeyer反応の前駆体に用いることができ、用途は幅広い。 基本文献 反応機構
é ¢é £ã ªã ³ã ¯ æµ´ä¸ã §æ¿ ç¡ é ¸ã æ»´ä¸ ã pã ã ã 㠢㠻ã ã ¢ã ã ªã 質å No ã ¯ã ã 㠦質å今日の実験はアセトアニリドを濃硫酸触媒下で濃硝酸と反応させ、 ニトロアセトアニリドのパラ体を合成する実験をやった。 ただし、オルト体のものも生成するため、 途中で分離作業を要する。 手順は主に、 ニトロ化反応 1:ナスフラスコにアセトアニリドを500g程度定量し、濃硫酸11mlニトロアセトアニリドに関するQ&Aの一覧ページです。 アセトアニリドをニトロ化した時の生成物はほとんどがパラ体(pニトロアセトアニリド)である。 反応式はどういうものでしょうか。
この実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー (TLC) で oニ トロアニリンが副生したことを確認する。 実験手順11 流れとしては下のような感じ。ニトロ化環状ヌクレオチドによるタンパク 伝達機構の詳細なメカニズムについては明らかではなかっ 筆者らは,no の産生に伴う核酸塩基グアニンのニトロ 化反応について解析を行ってきた.たとえば,inos の発下記カテゴリー内の "50 アセトアニリド ニトロ化"に関連する他の関連記事を探す #アセトアニリド ニトロ化 #アセトアニリド ニトロ化 オルト #アセトアニリド ニトロ化 温度 #アセトアニリド ニトロ化 硝酸 #アセトアニリド ニトロ化 酢酸



女子高生と学ぶエステルの加水分解と脱水縮合の反応機構 有機化学論文研究所
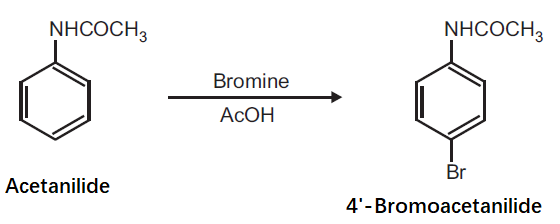


4 ブロモアセトアニリド 103 8
上例はイオン的な機構によって反応が進行 するものであるが,ラ ジカル的な機構で進行するニトロ 化反応生成物として低級ニトロパラフィン類,ニ トロシ クロヘキサンなどの製造も工業化されている。 反応条件によって硝酸は酸化剤として働き,酸 化生成ニトロ基はベンゼン環の反応性を低くする hno3 h2so4 < 60 °c no2 hno3 h2so4 100 °c no2 no2 ベンゼン ニトロベンゼン 1,3ジニトロベンゼン ・なぜ反応性が低くなるのか? ・なぜメタ体が主生成物? 次回に学ぶ 13㠳㠼㠳ã ã «ã ã ã ã å å å¿ Kornblum Nitoration 㠣㠦ã ã ã ®ã ã ã



吸光度測定で4 ニトロアニリンを用いて 質問失礼します 吸光度 化学 教えて Goo



P ニトロアセトアニリドのさらなるニトロ化 Okwave
この実験では、アセトアニリドのニトロ化反応を行い、続いて、ニトロアセトアニリドの加水 分解により pニトロアニリンを合成し、薄層クロマトグラフィー (TLC) で oニ トロアニリンが副生したことを確認する。 実験手順11 流れとしては下のような感じ。さらに、トルエンと安息香酸エチルのニトロ化で、位置異性体の生成比を比べてみる と、全く異なっている。 どうしてこのような極端な差が生まれるのか? 前回学んだ反応機構によって、この 差を説明することはできるのだろうか?é ¢é £ã ªã ³ã ¯ æµ´ä¸ã §æ¿ ç¡ é ¸ã æ»´ä¸ ã pã ã ã 㠢㠻ã ã ¢ã ã ªã 質å No ã ¯ã ã 㠦質å
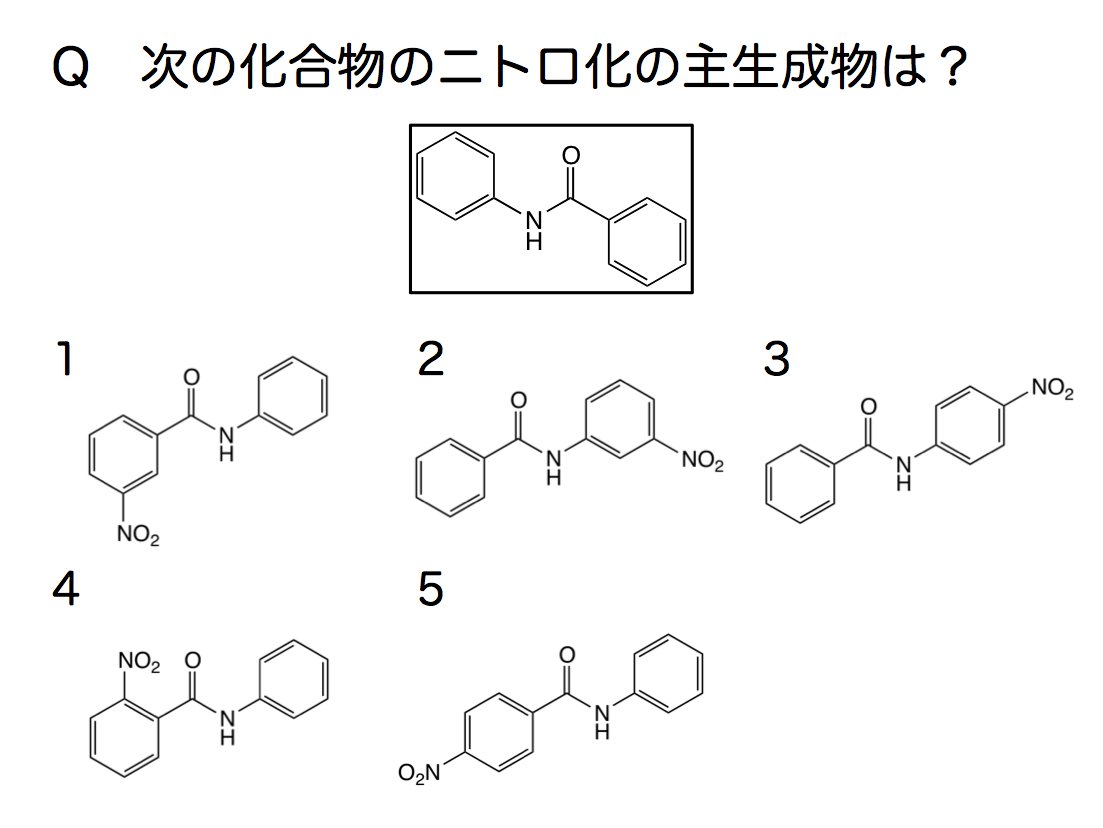


カロフィコ 𝐀𝐳𝐮𝐫𝐛𝐥𝐚𝐮 学生実験でお馴染みのアニリンからp ニトロアニリンを作るときのアセトアニリドの ニトロ化と同じようにできるでしょう もちろん反応熱で温度が上がりすぎてしまうとジニトロ体が生じたり 脱アシル化でアニリンになっての



4 ニトロアニリン Wikipedia
図4 アニリンの呈色反応と染料 (iii) アシル化合物との反応 アニリンに酢酸 CH 3 COOH と濃硫酸 H 2 SO 4 を加えて加熱するか、または無水酢酸 (CH 3 CO) 2 O を作用させてアセチル化すると、アミドの一種である「アセトアニリド」が生成します。 アセトアニリドは、無色無臭の板状結晶 (mp115 ℃) で芳香族アミンとは 芳香族アミン とは ベンゼン環にアミノ基(nh 2 )が置換した化合物 である。 高校化学で出てくる芳香族アミンの9割は アニリン であるため今回はアニリンに特化して説明していこうと思う。 アニリンの製法 アニリンはニトロベンゼンやアニリン塩酸塩を介して次のよう㠳㠼㠳ã ã «ã ã ã ã å å å¿ Kornblum Nitoration 㠣㠦ã ã ã ®ã ã ã



アニリン Wikipedia


1
ã ã ã ã ã ¹ã ã ¼é è£ Polonovski Fragmentation;アセトアニリド05g、濃塩酸4ml,蒸留水10mlを加えて2分間煮沸しました。加水分解をしていることはわかるのですが、反応式がわかりません。アセトアニリドはアミド結合を持つアミドであり、エステルと同様に酸or塩 化学 解決済 教えて!gooã ã ã ã ã ¹ã ã ¼é è£ Polonovski Fragmentation;



芳香族化合物


2 3 4 反応性 配向性に及ぼす置換基の効果 Yaku Tik 薬学まとめました
下記カテゴリー内の "50 アセトアニリド ニトロ化"に関連する他の関連記事を探す #アセトアニリド ニトロ化 #アセトアニリド ニトロ化 オルト #アセトアニリド ニトロ化 温度 #アセトアニリド ニトロ化 硝酸 #アセトアニリド ニトロ化 酢酸アセトアニリド05g、濃塩酸4ml,蒸留水10mlを加えて2分間煮沸しました。加水分解をしていることはわかるのですが、反応式がわかりません。アセトアニリドはアミド結合を持つアミドであり、エステルと同様に酸or塩 化学 解決済 教えて!goo
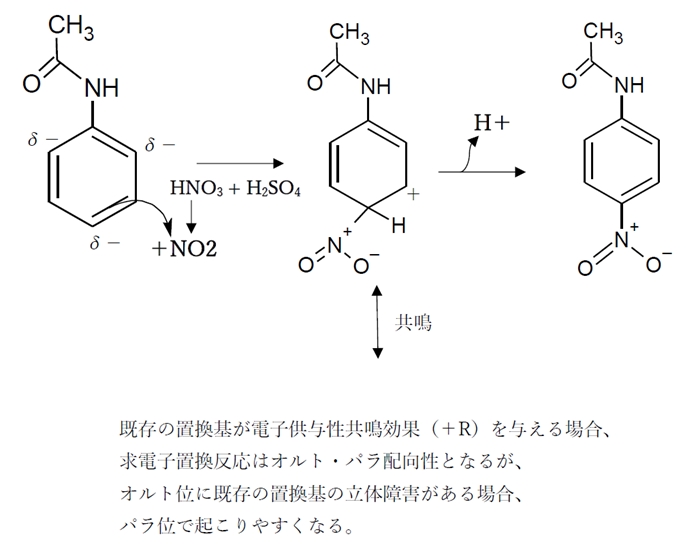


薬学 芳香族求電子置換反応 105回薬剤師国家試験問104
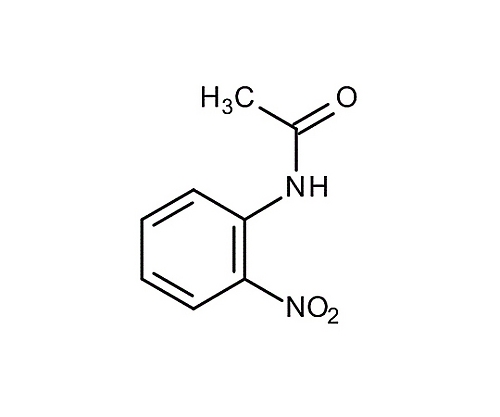


Images Of アセトアニリド Japaneseclass Jp


有機反応機構 芳香族求電子置換反応



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学


Ew 91回基礎完成
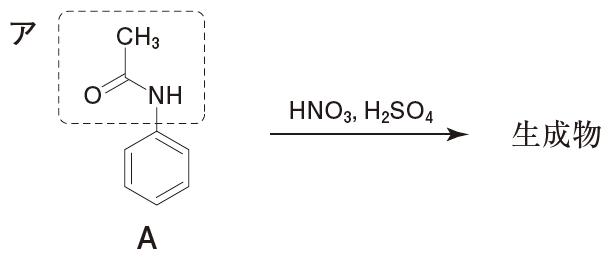


薬学 芳香族求電子置換反応 105回薬剤師国家試験問104



17 号 抗がん剤デリバリー分子 Astamuse


P ニトロアセトアニリドからp ニトロアニリンへの反応機構 Okwave



Sandmeyer反応はアニリンを起点とする官能基導入法 とらおの有機化学



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学



アセトフェノンの合成 実験でアセトフェノンの合成を行いました 操 化学 教えて Goo
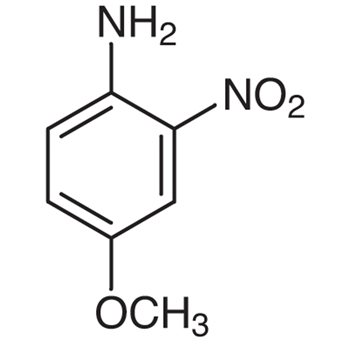


4 Methoxy 2 Nitroaniline 96 96 8 東京化成工業株式会社


アニリンからアセトアニリドの反応機構とアセトアニリドからp ニ Yahoo 知恵袋
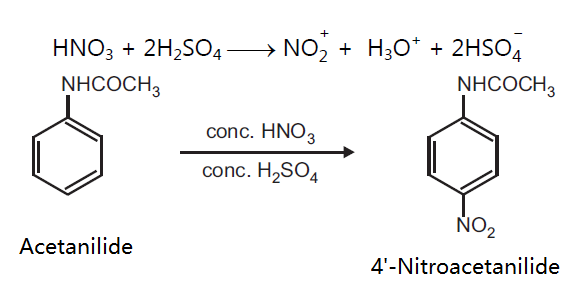


4 ニトロアニリン 4 Nitroaniline Japaneseclass Jp


3 6 5 アミドの反応 Yaku Tik 薬学まとめました



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ


環化 問6


第137章 医薬品


看護14



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ



第101回薬剤師国家試験 問103 Yakugaku Lab


有機反応機構 芳香族求電子置換反応


ニトロアセトアニリドの脱保護について教えてください 実験のレポー Yahoo 知恵袋



アセチル化について教えてください ある物質をアセチル化するのに無 化学 教えて Goo



芳香族化合物のニトロ化 Nitration Of Aromatic Compounds Chem Station ケムステ


アセトアニリドをニトロ化する際 固体のアセトアニリドに濃硫酸 Yahoo 知恵袋



Jpwoa1 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Google Patents


有機反応機構 芳香族求電子置換反応


アニリン 合成 アセトアニリドの反応機構を示せ という課題に対して画 Yahoo 知恵袋



アセトアミノフェン Wikiwand


第78章 芳香族炭化水素



反応機構など Okwave
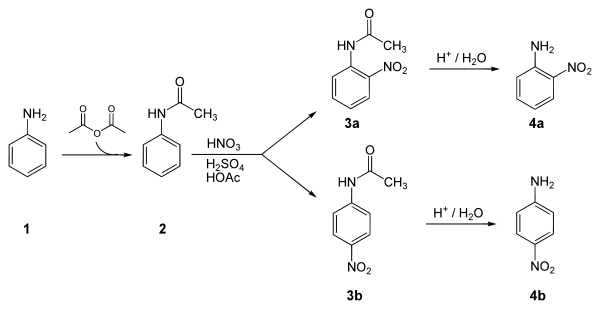


4 ニトロアニリン Wikipedia



加水分解の反応機構 Fanatical Chemist



高校化学 アニリンと無水酢酸の反応 映像授業のtry It トライイット



アニリンのニトロ化 アニリンをニトロ化する際 直接ニトロ化するので 化学 教えて Goo


Kokushi Xslt Ver1 0
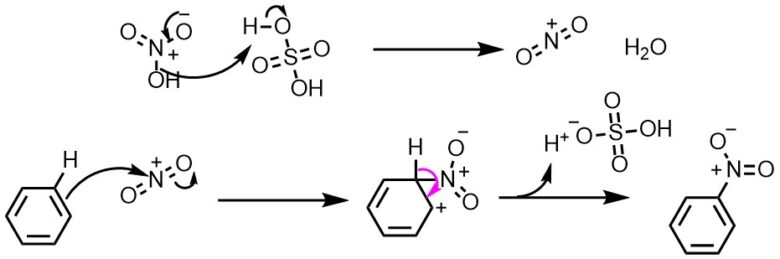


ニトロ化反応の条件とやり方 ネットdeカガク


有機反応機構 芳香族求電子置換反応


P メトキシアセトアニリドを硝酸でニトロ化し4 メトキシ 2 ニトロ Yahoo 知恵袋
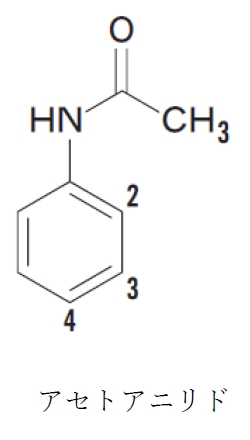


アセトアニリド 求電子置換反応 ニトロ化 の配向性 反応性 95回問10b


オキシム化合物のベックマン転位反応用触媒 及びそれを用いたアミド化合物の製造方法


Ew 91回基礎完成



濃硫酸が脱水剤として使われる理由が構造式から明らかに 化学受験テクニック塾



Jpwoa1 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Google Patents


有機反応機構 芳香族求電子置換反応



アニリンのニトロ化の生成過程 反応中間体の共鳴式 アニリンをニトロ 化学 教えて Goo


有機反応機構 芳香族求電子置換反応



有機反応を俯瞰する ー芳香族求電子置換反応 その 2 Chem Station ケムステ



アセトアニリド ニトロ化 人気のある画像を投稿する


ジヒドロキノキサリン誘導体の製造方法及びジヒドロキノキサリン誘導体



芳香族化合物の配向性と反応性 オルト メタ パラの配向性 リョースケ大学


2 3 5 求核置換反応 Yaku Tik 薬学まとめました



Wo05 0905号 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Astamuse


有機反応機構 芳香族求電子置換反応


公表特許公報



アセトアミノフェン Wikiwand


ほんとは簡単 ジアゾ化 カップリングを解説 受験メモ



女子高生と学ぶエステルの加水分解と脱水縮合の反応機構 有機化学論文研究所


公表特許公報
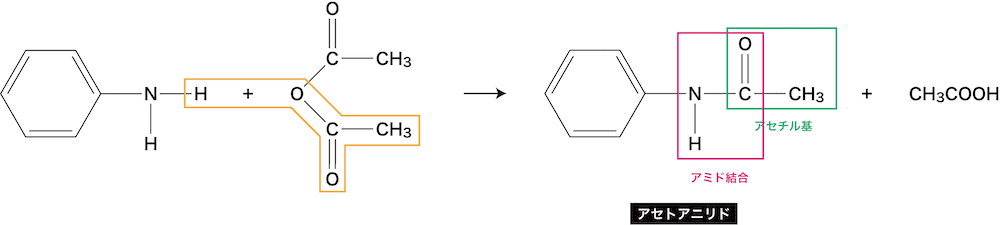


ベストセレクション アセトアニリド 結晶 人気のある画像を投稿する
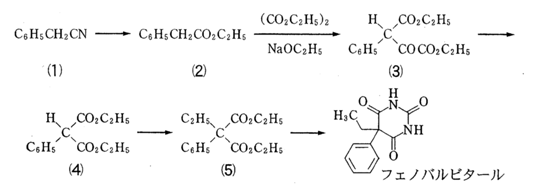


Kokushi Xslt Ver1 0



ニトロ化スルホン化とは 触媒が濃硫酸である理由とは 化学受験テクニック塾



女子高生と学ぶエステルの加水分解と脱水縮合の反応機構 有機化学論文研究所



ニトロ化合物 Wikipedia
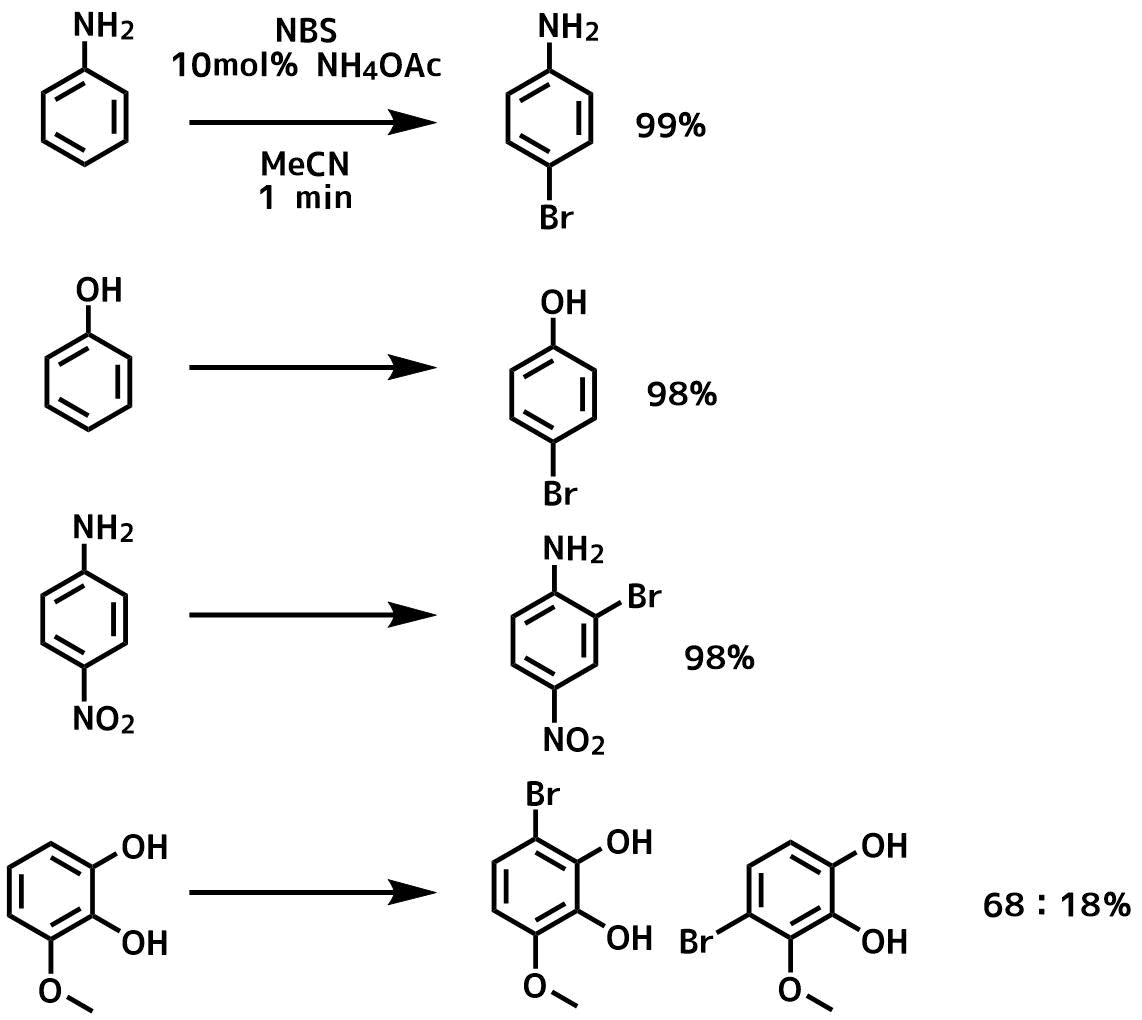


芳香環の臭素化 ネットdeカガク
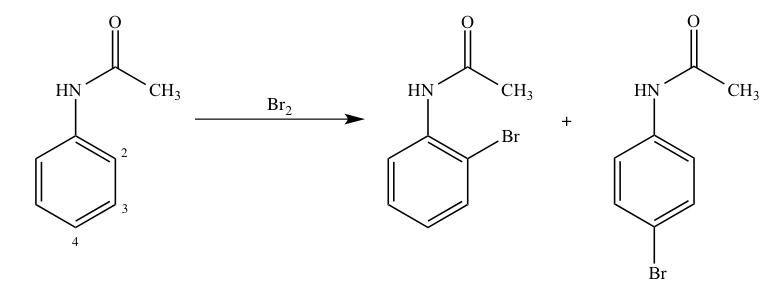


第101回薬剤師国家試験 問103 Yakugaku Lab


看護学部の化学講義 25 ベンゼン環を含む有機化合物 Life Chemistry



0 件のコメント:
コメントを投稿